Síntese e caracterização de hidroxissais lamelares de zinco intercalados com antocianinas extraídas da uva BRS Magna
DOI:
https://doi.org/10.14295/vetor.v34i2.18105Palavras-chave:
Antocianinas, BRS Magna, Corantes naturais, Hidroxissais lamelares de zinco, Troca aniônicaResumo
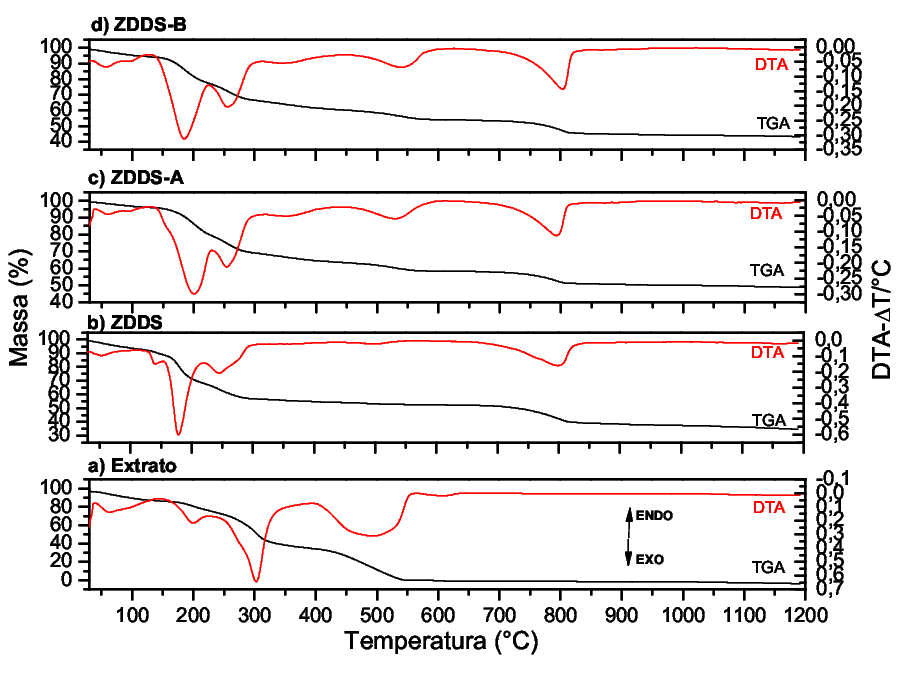
O estudo e a aplicação de corantes naturais têm ganhado crescente relevância devido à demanda por alternativas sustentáveis e menos tóxicas em relação aos corantes e pigmentos sintéticos. Neste trabalho, foram sintetizados e caracterizados hidroxissais lamelares de zinco (HSL) intercalados com antocianinas extraídas da uva BRS Magna, com o objetivo de melhorar a estabilidade desses compostos. Os HSL são materiais capazes de promover interações entre a matriz inorgânica (lamelas) e espécies orgânicas, resultando em propriedades distintas das dos precursores e possibilitando novas aplicações para o material híbrido. O processo envolveu a preparação de um extrato de antocianinas, seguido da síntese dos precursores dos HSL por co-precipitação. Posteriormente, a intercalação das antocianinas foi realizada por meio de troca aniônica, seguida da caracterização dos materiais obtidos. A formação dos HSL foi confirmada por difratometria de raios X (DRX) pelo deslocamento de alguns picos, e a espectroscopia de infravermelho com transformada de Fourier (FTIR) evidenciou a intercalação das antocianinas devido a presença de vibrações características. Análises termogravimétrica (TGA) e térmica diferencial (DTA) revelaram mudanças no perfil de estabilidade térmica dos materiais híbridos. Os resultados indicam o potencial dos HSL de zinco como matrizes estabilizadoras de antocianinas, promovendo o desenvolvimento de novos materiais pigmentários com possíveis aplicações em diversas áreas.
Downloads
Referências
P. B. L. Constant, A. Borges, T. Nunes, F. da Silva, A. da Silva, V. de lima, M. Ferreira, e P. Stringheta, “Aplicação do corante de açaí (Euterpe oleracea M) em sistemas alimentícios,” Observatório de la Economia Latinoamericana, vol. 21, no. 11, pp. 18571–18593, 2023. Disponível em: Https://doi.org/10.55905/oelv21n11-001
P. Mpountoukas, A. Pantazaki, E. Kostareli, P. Christodoulou, D. Kareli, S. Poliliou, C. Mourelatos, V. Lambropoulou, e T. Lialiaris, “Cytogenetic evaluation and DNA interaction studies of the food colorants amaranth, erythrosine and tartrazine,” Food and Chemical Toxicology, vol. 48, no. 10, pp. 2934–2944, 2010. Disponível em: https://doi.org/10.1016/j.fct.2010.07.030
M. A. Prado, e H. T. Godoy, “Corantes artificiais em alimentos,” Alimentos e Nutrição, vol. 14, n. 2, pp. 237-250, 2009.
T. J. Lopes, M. F. Xavier, M. G. N. Quadri, e M. B. Quadri, “Antocianinas: uma breve revisão das características estruturais e da estabilidade,” Revista Brasileira de Agrociência, vol. 13, no. 3, pp. 291–297, 2007. Disponível em: https://periodicos.ufpel.edu.br/index.php/CAST/article/view/1375
L. B. Anastácio, D. A. Oliveira, C. R. Delmaschio, L. M. G. Antunes, e F. M. D. Chequer, “Corantes alimentícios amaranto, eritrosina B e tartrazina, e seus possíveis efeitos maléficos à saúde humana,” Journal of Applied Pharmaceutical Sciences, vol. 2, no. 3, pp. 16–30, 2016. Disponível em: http://hdl.handle.net/1843/39736
R. B. Kanarek, “Artificial food dyes and attention deficit hyperactivity disorder,” Nutrition Reviews, vol. 69, no. 7, pp. 385–391, 2011. Disponível em: https://doi.org/10.1111/j.1753-4887.2011.00385.x
N. S. Santos, F. L. A. T. da Silva, e M. T. S. L. Neta, “Corantes naturais: importância e fontes de obtenção,” RECIMA21 - Revista Científica Multidisciplinar, vol. 3, no. 3, pp. 1-15, 2022, Disponível em: https://doi.org/10.47820/recima21.v3i3.1165
F. Delgado-Vargas, A. R. Jiménez, e O. Paredes-López, “Natural pigments: carotenoids, anthocyanins, and betalains - characteristics, biosynthesis, processing, and stability,” Critical Reviews in Food Science and Nutrition, vol. 40, no. 3, pp. 173–289, 2000. Disponível em: https://doi.org/10.1080/10408690091189257
D. Li, P. Wang, Y. Luo, M. Zhao, e F. Chen, “Health benefits of anthocyanins and molecular mechanisms: update from recent decade,” Critical Reviews in Food Science and Nutrition, vol. 57, no. 8, pp. 1729–1741, 2017. Disponível em: https://doi.org/10.1080/10408398.2015.1030064
L. C. Marquart, “Über die Farben der Blüthen,” Archiv der Pharmazie, vol. 56, no. 3, pp. 244–265, 1836. Disponível em: https://doi.org/10.1002/ardp.18360560305
P. Bridle e C. F. Timberlake, “Anthocyanins as natural food colours - selected aspects,” Food Chemistry, vol. 58, no. 1–2, pp. 103–109, 1997. Disponível em: https://doi.org/10.1016/S0308-8146(96)00222-1
J. B. Harborne, The flavonoids advances in research since 1986, 1st ed. New York, United States of America: Routledge, 2017. Disponível em: https://doi.org/10.1201/9780203736692
J. F. Gonnet, “Colour effects of co-pigmentation of anthocyanins revisited-1. A colorimetric definition using the CIELAB scale,” Food Chemistry, vol. 63, no. 3, pp. 409–415, 1998. Disponível em: https://10.1016/S0308-8146(98)00053-3
G. Mazza, Anthocyanins in Fruits, Vegetables, and Grains, 1st ed. Boca Raton, United States of America: CRC Press, 2017. Disponível em: https://doi.org/10.1201/9781351069700
U. Mathesius, “Flavonoid functions in plants and their interactions with other organisms,” Plants, vol. 7, no. 2, p. 30-33, 2018. Disponível em: https://doi.org/10.3390/plants7020030
D. Ghosh e T. Konishi, “Anthocyanins and anthocyanin-rich extracts: role in diabetes and eye function,” Asia Pacific Journal of Clinical Nutrition, vol. 16, no. 2, pp. 200–208, 2007. Disponível em: https://pubmed.ncbi.nlm.nih.gov/17468073/
K. Filipiak, M. Hidalgo, J. M. Silvan, B. Fabre, R. J. Carbajo, A. Pineda-Lucena, A. Ramos, B. Pascual-Teresa, e S. Pascual-Teresa, “Dietary gallic acid and anthocyanin cytotoxicity on human fibrosarcoma HT1080 cells. A study on the mode of action,” Food & Function, vol. 5, no. 2, pp. 381–389, 2014. Disponível em: https://10.1039/C3FO60465A
C. Manach, A. Scalbert, C. Morand, C. Rémésy, e L. Jiménez, “Polyphenols: food sources and bioavailability,” The American Journal of Clinical Nutrition, vol. 79, no. 5, pp. 727–747, 2004. Disponível em: https://doi.org/10.1093/ajcn/79.5.727
P. H. Março, R. J. Poppi, I. S. Scarminio, e R. Tauler, “Investigation of the pH effect and UV radiation on kinetic degradation of anthocyanin mixtures extracted from Hibiscus acetosella,” Food Chemistry, vol. 125, no. 3, pp. 1020–1027, 2011. Disponível em: https://doi.org/10.1016/j.foodchem.2010.10.005
G. G. C. Arizaga, K. G. Satyanarayana, e F. Wypych, “Layered hydroxide salts: Synthesis, properties and potential applications,” Solid State Ionics, vol. 178, no. 15–18, pp. 1143–1162, 2007. Disponível em: https://doi.org/10.1016/j.ssi.2007.04.016
Y. Kohno, R. Kinoshita, S. Ikoma, e K. Yoda, “Stabilization of natural anthocyanin by intercalation into montmorillonite,” Applied Clay Science, vol. 42, no. 3–4, pp. 519–523, 2009. Disponível em: https://doi.org/10.1016/j.clay.2008.06.012
T. Matsukura e H. Tanaka, “Applicability of zinc complex of L-carnosine for medical use,” Biochemistry, vol. 65, no. 7, pp. 817–823, 2000. Disponível em: http://europepmc.org/abstract/MED/10951100
C. Delhoyo, “Layered double hydroxides and human health: An overview,” Applied Clay Science, vol. 36, no. 1–3, pp. 103–121, 2007. Disponível em: https://doi.org/10.1016/j.clay.2006.06.010
J. Demel, J. Pleštil, P. Bezdička, P. Janda, M. Klementová, e K. Lang, “Layered zinc hydroxide salts: Delamination, preferred orientation of hydroxide lamellae, and formation of ZnO nanodiscs,” Journal of Colloid and Interface Science, vol. 360, no. 2, pp. 532–539, 2011. Disponível em: https://doi.org/10.1016/j.jcis.2011.04.024
S. A. Maruyama, S. R. Tavares, A. A. Leitão, e F. Wypych, “Intercalation of indigo carmine anions into zinc hydroxide salt: A novel alternative blue pigment,” Dyes and Pigments, vol. 128, pp. 158–164, 2016. Disponível em: https://doi.org/10.1016/j.dyepig.2016.01.022
J. Miao, M. Xue, H. Itoh, e Q. Feng, “Hydrothermal synthesis of layered hydroxide zinc benzoate compounds and their exfoliation reactions,” Journal of Materials Chemistry, vol. 16, no. 5, pp. 474–480, 2006. Disponível em: https://doi.org/10.1039/B511110B
J. Liu, Y. Zhang, e X. Zhang, “Inorganic–organic nanohybrid materials of layered zinc hydroxide nitrate with intercalated salicylate: preparation, characterization and UV-blocking properties,” International Journal of Nanoscience, vol. 15, no. 01n02, pp. 1650010-1–1650010-9, 2016. Disponível em: https://doi.org/10.1142/S0219581X16500101
S. Jaerger, D. A. de Ramos Nogueira, D. S. de Oliveira, M. V. Machado, e R. Marangoni, “Study of different morphology of Zzinc hydroxide salt as adsorbent of azo dyes,” ChemistrySelect, vol. 6, no. 17, pp. 4354–4367, 2021. Disponível em: https://doi.org/10.1002/slct.202100730
M. R. E. Arruda, E. K. S. Barbosa, C. F. Silva, e G. M. Vinhas, “Avaliação de extratos de antocianinas como indicadores de pH obtidos por diferentes métodos,” Brazilian Journal of Food Research, vol. 10, no. 3, p. 87, 2019. Disponível em: https://doi.org/10.3895/rebrapa.v10n3.10942
L. I. L. Favaro, V. M. Balcão, L. K. H. Rocha, E. C. Silva, J. M. Oliveira Jr., M. M. D. C. Vila, e M. Tubino, “Physicochemical characterization of a crude anthocyanin extract from the fruits of jussara (Euterpe edulis Martius): Potential for food and pharmaceutical applications,” Journal of the Brazilian Chemical Society, vol. 20, no. 10 pp. 2072-2088, 2018. Disponível em: https://doi.org/10.21577/0103-5053.20180082
D. Dupeyrón, M. Kawakami, J. Rieumont, e J. Carvalho, “Formulation and characterization of anthocyanins-loaded nanoparticles,” Current Drug Delivery, vol. 14, no. 1, pp. 54–64, 2017. Disponível em: https://doi.org/10.2174/1567201813666160915102151
H. Chang, M. J. Kao, T. L. Chen, C. H. Chen, K. C. Cho, e X. R. Lai, “Characterization of natural dye extracted from wormwood and purple cabbage for dye-sensitized solar cells,” International Journal of Photoenergy, vol. 2013, pp. 1–8, 2013. Disponível em: https://doi.org/10.1155/2013/159502
D. L. Pavia, G. M. Lampman, G. S. Kriz, e J. A. Vyvyan, Introduction to Spectroscopy, 4th ed. Belmont, United States of America: Cengage Learning, 2008.
J. W. Lee, W. C. Choi, e J.D. Kim, “Size-controlled layered zinc hydroxide intercalated with dodecyl sulfate: effect of alcohol type on dodecyl sulfate template,” CrystEngComm, vol. 12, no. 10, pp. 3249-3254, 2010. Disponível em: http://doi.org/10.1039/c002296a
A. Elsayed, M. Al-Remawi, N. Qinna, A. Farouk, K. A. Al-Sou’od, e A. A. Badwan, “Chitosan–sodium lauryl sulfate nanoparticles as a carrier system for the in vivo delivery of oral insulin,” AAPS PharmSciTech, vol. 12, no. 3, pp. 958-964, 2011. Disponível em: https://doi.org/10.1208/s12249-011-9647-5
G. Hardinasinta, M. Mursalim, J. Muhidong, e S. Salengke, “Degradation kinetics of anthocyanin, flavonoid, and total phenol in bignay (Antidesma bunius) fruit juice during ohmic heating,” Food Science and Technology, vol. 42, n, e64020, pp. 1-11, 2022. Disponível em: https://doi.org/10.1590/fst.64020
S. Jaerger, A. Zimmermann, S. F. ZawadzkiI, F. Wypych, e S. C. Amico, “Zinc layered hydroxide salts: intercalation and incorporation into low-density polyethylene,” Polímeros, vol. 24, no. 6, pp. 673–682, 2014. Disponível em: https://doi.org/10.1590/0104-1428.1733